外周 T 细胞淋巴瘤(peripheral T - cell lymphomas,PTCLs)是指起源于成熟 T 细胞和自然杀伤细胞的一组生物学特性和分子特征方面异质性较大的恶性肿瘤,除皮肤 T 细胞淋巴瘤较惰性外,其余类型 PTCLs 均表现为侵袭性。PTCLs 占侵袭性非霍奇金淋巴瘤(NHL)的 15%–20%,与侵袭性 B 细胞淋巴瘤相比,PTCLs 接受标准化疗的预后较差。
WHO 分类更新
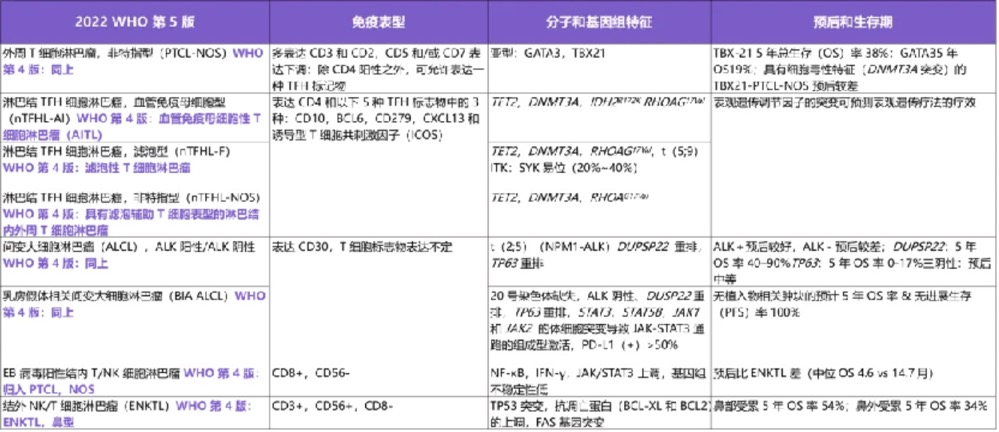
根据临床和病理特征以及来自全基因组测序研究的最新分子生物学数据,2022 年 WHO 淋巴造血组织肿瘤分类第五版(WHO - HAEM5)对 PTCL 进行了细化分类(表 1)。
表 1. 常见 PTCL 亚型的分类更新
风险分层及预后评估
外周 T 细胞淋巴瘤存在较大的异质性,其预后与多种因素有关,寻找有效的预后模型对不同危险度患者进行分层,并依此而给予不同强度的治疗成为一些机构的研究目标。目前在 PTCLs 中运用较为普遍的预后模型包括:
(1)国际预后指数(IPI):由年龄、血清乳酸脱氢酶、行为状况评分(PS 评分)、Ann Arbor 分期和结外受累器官数目 5 个要素组成;对判断大多数 NHL 的预后,尤其是弥漫大 B 细胞淋巴瘤取得良好成效。一些研究显示,IPI 评分在 PTCLs 的预后评价中也有重要价值。
(2)外周 T 细胞淋巴瘤非特异型预后指数(PIT):2004 年,一项来自意大利的多中心回顾性研究提出骨髓受侵是 PTCL—NOS 的重要预后因素,并以此为基础提出新的预后指数 PIT(年龄>60 岁、血清 LDH、PS 评分、骨髓是否受侵)。该预后模型能将患者从低危到高危组分为四组,各组 5 年 OS 率分别为 62%、53%、33%和 18%,具有良好的区分度。
(3)修订的 PIT(mPlT):Went 等考虑病理因素后,对 PIT 进行修订,利用 Ki - 67 ≥ 80%替代骨髓受侵,命名为 mPIT 模型,并认为在预后预测上优于 PIT。
(4)国际外周 T 细胞淋巴瘤项目评分(IPTCLP):由国际外周 T 细胞淋巴瘤项目组提出,适用于 PTCL - NOS 和 AITL。该模型仅包括年龄、PS 评分和血小板计数 3 个因素。
后续的一些研究对 IPI、PIT、mPIT 以及 IPTCLP 在 PTCLs 中预后预测价值进行了评价,但并未得一致的结论。目前在临床工作中对 PTCLs 预后评价应用最为广泛的仍然是 IPI 评分和 PIT 评分。
治疗进展
目前 PTCL —线治疗方案常采用以蒽环类药物或吉西他滨为基础的化疗方案,治疗总体缓解率(ORR)为 70%~80%,但 50%~70 %的患者出现复发进展。传统化疗挽救性治疗复发难治(R/R)PTCL 的疗效较差,中位 OS 仅数月。R/R 患者可考虑行异基因造血干细胞移植,但治疗相关死亡风险较高。随着对 PCTLs 分子生物学研究的持续深入,靶向、免疫治疗的发展使 PTCL 的疗效取得良好进步。
一线治疗
含蒽环类药物的化疗方案如 CHOP(环磷酰胺、阿霉素、长春新碱和强的松)或CHOP 样方案是 PTCLs 最常使用的一线方案,完全缓解(CR)率及 3 年 OS 率分别为 39% 和 26%,显著差于 B - NHL(67% 和 50%)。
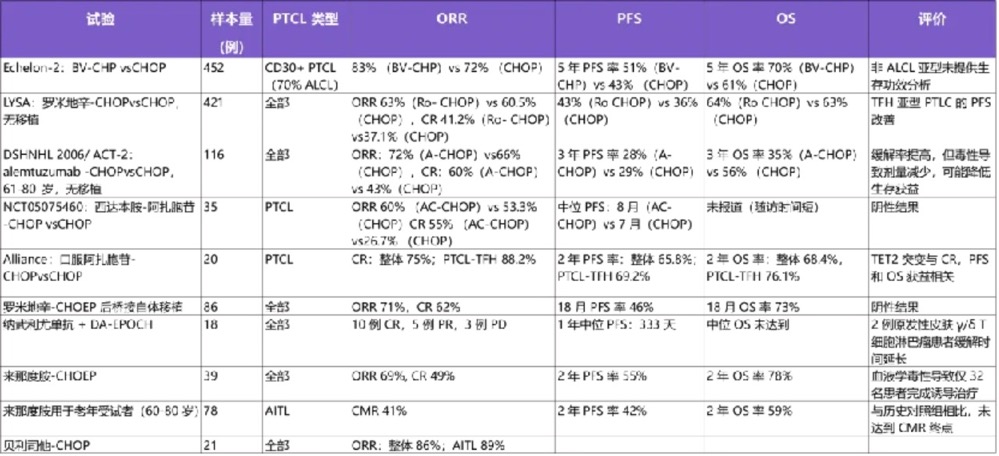
最近多项研究报道了初诊 PTCL 的治疗进展,主要涉及新化疗方案的探索、单克隆抗体、表观遗传疗法、自体干细胞移植(ASCT)(表 2)。部分治疗方案已纳入最新版的中国临床肿瘤学会(CSCO) PTCL 治疗指南(表 3)。
表 2. PTCL 初始治疗的临床试验结果汇总
表 3. 2023 CSCO 对 PTCL 的初始治疗的治疗推荐
抗体偶联药物(ADC)
维布妥昔单抗(BV)是一种靶向 CD30 抗体偶联药物。BV 联合化疗(A + CHP)优于单纯化疗(CHOP),中位 PFS 为 48 个月 vs 21 个月(HR 0.71),复发风险降低 29%。5 年随访显示反应的持久性,接受 BV - CHP 和 CHOP 的患者的 PFS/OS 率分别为 51%/70% vs 43%/61%。在非 ALCL 亚型中,亚组分析报告 PFS HR 0.96(95%CI 0.63 - 1.47),且药物耐受性良好,安全性可控。基于该结果,2019 年美国国家癌症综合网络(NCCN)指南更新 PTCL 一线治疗推荐, ALCL 优选 BV + CHP 方案,也推荐于其他任何 CD30 + 的组织学亚型。美国食品药品监督管理局(FDA)也将 BV 作为 CD30 阳性 PTCL 患者的一线治疗选择。
表观遗传疗法
表观遗传学修饰是指在不改变 DNA 序列的基础上对基因表达的调节方式。PTCL 患者多见表观遗传调控异常,如 DNA 甲基化、组蛋白修饰、染色质重塑等。目前已有的表观遗传学调控药物包括去甲基化药物(HMA)如阿扎胞苷、地西他滨,组蛋白去乙酰化酶抑制剂(HDACi)如西达苯胺、罗米地辛等。
口服阿扎胞苷(CC - 486)是一种低甲基化药物。在 CHOP 前联合口服阿扎胞苷用于 PCTL 初始治疗的单臂 II 期临床试验显示,可评价疗效的 20 位受试者中,ORR(≥ CR)高达 75%,2 年 PFS 率 69%,OS 率 76.1%,与单独使用 CHOP 的历史数据相比有明显改善。
罗米地辛(Romidepsin)是一种 HDACi,与 DNA 甲基转移酶抑制剂具有协同作用,疗效明显优于单一新药治疗。近期研究采用罗米地辛 + 5 - 氮杂胞苷联合给药,在 PTCLs 中 ORR 达 73%,CR 55%。
免疫调节剂
来那度胺作为一种具有抗肿瘤特性的免疫调节剂,主要作用包括肿瘤细胞毒性、免疫调节、抗血管生成特性以及通过增强免疫突触形成来增强 NK/T 细胞功能。
一项 CHOEP 方案联合来那度胺用于初诊 PTCL 的研究中,30 例患者完成 6 个周期治疗,CR 和 ORR 分别为 63% 和 48%,预估 1 年 PFS 和 OS 分别为 68%和 89%,终止率为 15%。
大剂量化疗联合造血干细胞移植(HSCT)
目前的 NCCN 指南推荐 ASCT 巩固治疗作为除 ALK + ALCL 外其他组织学亚型 PTCLs 患者化疗后 CR1 期的首选。ALK + ALCL 预后较好,不推荐进行 CR1 期移植,但高 IPI 评分患者除外。高风险患者 CR1 期也可以选择自体造血干细胞移植(allo - HSCT)。